张启国医生的科普号
- 精选 中华骨髓库检索流程
1. 患者做HLA高分辨检测(3000元/人):患者本人抽血(血常规管,5~10ml)进行HLA高分辨检测,建议直接送中华骨髓库指定的HLA高分辨检测实验室,一般2周内出结果。目前全国有6个实验室,分别是:北京红十字血液中心HLA高分辨分型确认实验室黑龙江省血液中心HLA高分辨分型确认实验室陕西省血液中心HLA高分辨分型确认实验室浙江省血液中心HLA高分辨分型确认实验室苏州中心血站/苏州大学附属第一医院HLA高分辨分型确认实验室深圳市血液中心HLA高分辨分型确认实验室2. 中华骨髓库检索(免费):联系具有中华骨髓库造血干细胞移植资质的医院,请血液科医生将患者的HLA配型结果及患者的个人信息输入中华骨髓库网站。信息输入后,中华骨髓库工作人员将审核信息,并将患者HLA配型结果与骨髓库捐献者数据库比对,筛选出与患者HLA配型初步相合的志愿者,发出配型报告单。此时,每个患者将会有一个骨髓库编号。患者可以登录中国造血干细胞捐献者资料库(中华骨髓库)网站www.cmdp.org.cn了解相关信息。3. 中华骨髓库联系捐献者确认捐献意愿移植医院的医生将患者对应的志愿捐献者列表,进行捐献者的排序。随后,中华骨髓库各地区分库工作人员将联系捐献者,确认捐献意愿。这个过程可能比较长,其实站在捐献者和捐献者家人的角度,这是完全可以理解的。4. 捐献者高分辨检测(3000元/人份)捐献者同意后,中华骨髓库将会发出 “高分辨通知单”,其实就是捐献者高分辨缴费通知单。通知单上有患者姓名、骨髓库编号、捐献者编号、血样寄送的HLA高分辨检测实验室地址、电话、银行账号等信息。如果患者此前的HLA高分辨检测不是在上面6个实验室做的,那么需要抽血重新送检。捐献者的高分辨检测费由患者支付。患者付费后,需要告知医生。骨髓库工作人员随后将安排捐献者抽血、寄送血样到指定高分辨实验室。从缴费到HLA高分辨结果出来一般需要大约1个月的时间。如果初步配型相合的捐献者比较多,中华骨髓库一般会同时动员2~3个捐献者。同时做多个捐献者的HLA高分辨检测,将能节约患者等待移植的时间。5. 捐献者体检(20000元)捐献者与患者HLA配型符合移植要求后,骨髓库将安排捐献者到中华骨髓库指定的造血干细胞采集医院做全身体检。这个过程一般需要大约1个月的时间。体检结果的有效期为3个月,如果超过3个月做移植,骨髓库需要安排捐献者重新体检。捐献者体检费由中华骨髓库代收。6. 安排移植时间捐献者体检合格后,移植医院的医生将根据患者情况,通过中华骨髓库工作人员与捐献者沟通,确认移植日期。7. 造血干细胞捐献、采集、运送(30000元左右)移植前,移植医院为患者制定移植计划,随后采集医院为捐献者制定外周血造血干细胞的采集计划。此时,患者需要将捐献者的造血干细胞采集费通过银行汇款到采集医院。捐献者的造血干细胞将由移植医院的医疗人员当天取回。从患者第一次交纳捐献者高分辨费用开始,到移植一般需要至少3~4个月的时间。因此,如果疾病情况需要移植,请患者尽早联系移植医院的医生进行中华骨髓库的配型检索工作。在等待移植的这段时间里,患者仍需要继续治疗,患者本人也需要进行移植前的全身体检,并与移植医院的医生保持沟通,让医生了解患者的疾病状况。截止2020年12月,中华骨髓库有近300万志愿捐献者,患者检索配型成功并进行移植的概率大约为10%。对于在中华骨髓库检索不到HLA配型相合志愿者的患者,还可以申请到台湾佛教慈济干细胞中心进行检索,台湾佛教慈济骨髓库有大约28万志愿捐献者。目前,志愿捐献者的队伍还在不断扩大,患者配型成功的概率将会更高。在中华骨髓库的配型检索过程中,患者需要理解的是:中华骨髓库及各地区分库的工作人员做了很多幕后工作,没有他们与捐献者、移植医院、采集医院的反复沟通与真诚服务,造血干细胞移植无法顺利进行。当然,患者最应当感激的是骨髓库的志愿捐献者,没有他们的无私奉献,患者无法获得第二次生命!上海市第一人民医院/上海交通大学附属第一人民医院是中华骨髓库和台湾佛教慈济骨髓库第一批指定的造血干细胞移植医院和采集医院。我院血液科万理萍主任医师负责中华骨髓库和台湾佛教慈济骨髓库的检索、配型工作。需要联系配型的患者可以登录万理萍医生的个人网站wanliping01.haodf.com,进行网上咨询或者申请电话咨询,还可以手机下载 “掌上市一”App或者登陆上海市第一人民医院网站www.firsthospital.cn,预约万理萍医生的专家门诊(周一上午、周二下午)。本文系万理萍医生授权好大夫在线(www.haodf.com)发布,未经授权请勿转载。
万理萍 主任医师 上海市第一人民医院(南部) 血液科2.1万人已读 - 引用 化疗期间如何缓减副作用
在临床上大多数血液肿瘤患者都会问到同样的问题,就是化疗期间怎么缓减恶心呕吐等副作用,下面我就以化疗期间饮食为题,给大家一些建议。1、化疗前增强体质,增加营养化疗的效果与病人体质的强弱、营养状况有明显关系。如果营养水平差、体质不好则化疗效果差,副反应也就大。因此化疗前总体要求是增强体质,增加营养。多摄入蛋白质。选用能补益气血,健脾补肾的食品,如芝麻、龙眼、菠菜、鸡、鸭、猪肉、牛肉、鱼、豆制品、蛋、奶类等。2、易消化食物,增加食欲,防治呕吐化疗时病人出现食欲减退、恶心、呕吐、腹泻等症状,给他的食物要易于消化,主食以流汁或半流汁为主,比如,五谷粥、面条等。还可以采取更换食谱,改变烹调方法,增加食物的色、香、味;少量多餐,吃一些清淡爽口的生拌凉菜;在饮食中可加入一些生姜,以止呕;也可用药膳开胃健脾,如山楂肉丁、黄芪、山药、萝卜、白扁豆、香蕈、陈皮等。3、富含铁质的食物,缓解头晕乏力在化疗的过程中,病人的白细胞和血小板会下降,出现头昏,倦怠乏力,心慌气短,脱发等表现,这时选择富含铁质的食物,可以供给身体足够造血原料,如猪肝、瘦肉、鱼、菠菜、金针菜、桂圆等。4、多吃蔬菜水果,补充营养提高免疫在饮食调理上要注意补充足够的优质蛋白,动物蛋白以低脂肪的鸡、鱼、奶为好,是吃含植物蛋白丰富的豆类食品,可选用人参、西洋参、红枣、膳鱼、甲鱼、桂圆等。癌症病人每天需 5~10 克维生素C,以支持白血球和红血球的功能,并预防化疗药物产生的副作用。最好将含维生素C多的蔬菜,水果榨汁饮用为了防止呕吐,饮食以清淡而富有营养易于消化的食物为主,可多吃些新鲜蔬菜,水果,采取少吃多餐的方法。化疗期间注意事项:一、注意定期复查血常规。化疗可能引起不同程度的血细胞减少,当白细胞减少时,身体抵抗力下降,应避免去人多的地方并严格控制探视人数,以免增加细菌或病毒感染的机会;血小板减少时,凝血功能下降,容易引起出血,应避免撞伤,用软毛刷刷牙,避免进食粗糙食物,皮肤有出血点时应及时告诉医生。二、病人及家属应了解所用化疗药物的常见不良反应。除常见的消化道不良反应外,很多化疗药物在静脉注射时若漏在血管外可引起局部红肿,严重者出现糜烂、坏死、病人疼痛难忍。因此家属及病人需密切观察穿刺部位,发现局部肿胀、漏液等现象,应及时向医务人员反映。
包慎 主任医师 宁夏人民医院 血液内科5039人已读 - 引用 移植后管理丨造血干细胞移植后院外注意事项
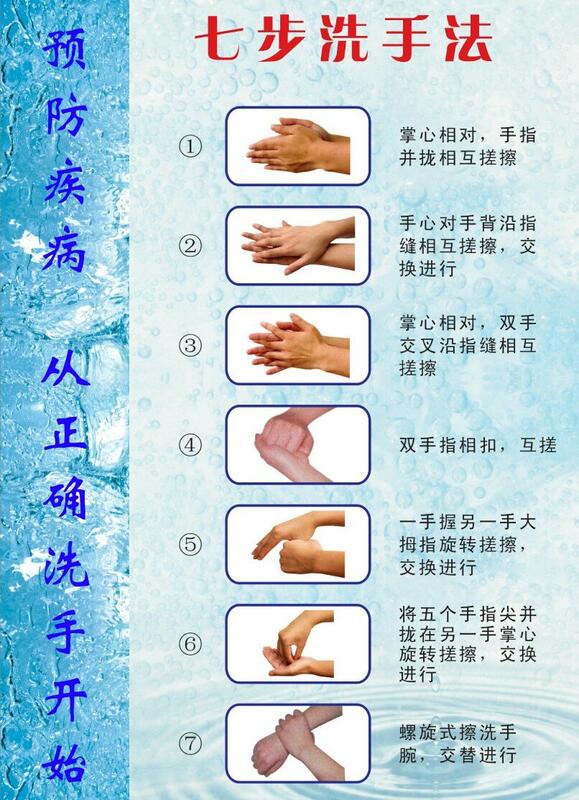
亲!您已经完成造血干细胞移植,顺利出仓,走过移植的第一步。完事开头难,我们理解您承受的千辛万苦您已经顺利,理解您出院后兴奋的心情。但目前您离移植成功仍有很长的距离,可以说是“万里长征才走过一千里”。亲,请注意:您现在是一个“玻璃人”——抵抗力非常低下。为了您院外期间的幸福安康,请管好自己的“眼、口、手、脚”,并选择一个干净通风的环境居住。俗话说,病从口入,管理好自己的饮食,就可以避免一些经食物传播的疾病。为了您的健康,请亲们做到以下几点:①注意饮食卫生,清淡,富营养饮食,勿暴饮暴食;②使用现做的食物,忌用隔顿、隔夜的食物;③不提倡饮用液体奶,特别是酸奶等,可食用固体奶粉,例如安素粉等;④若中性粒细胞大于2G/L,可食用当季水果,但要注意清洁卫生;⑤移植后1-2年内禁用冬虫夏草、人参、灵芝等;⑥不提倡外出饭店、餐馆等地就餐;⑦严格按照医嘱服用药物,建议环孢素A等免疫抑制剂在早8点晚20点和食物同服;当有抽血查环孢素A/他克莫司浓度或伏立康唑浓度时,请在当天抽血后服用。俗话说“眼观六路,耳听八方”。移植后有许多并发症,需要患者密切观察记录病情,因此,亲们,移植后请练就一双“火眼金睛”,仔细观察记录院外期间相关并发症的表现:①首先要明确有无发热,自己学会测量体温,若体温大于38℃,需及时就诊;②仔细观察自己的皮肤及眼睛颜色变化、有无皮疹,若出现皮肤、眼睛明显变黄,皮肤出现疹子、瘙痒、皮肤变硬、关节活动受限等,需记录时间,并及时就诊;③若出现“拉肚子”、“肚子疼”,特别是每天大便次数大于3次或出现稀水样、墨绿色大便时,请尽早找到你的主诊医生,尽早处理,否则将会造成严重后果;④注意自己的嘴巴,时常使用小镜子观察,若出现嘴唇泛白、脱皮,嘴巴内疼痛、溃烂、白斑等,需尽快求助你的主诊医生;⑤细心观察自己的尿液否变黄、变红、有较多的泡沫等,以及是否存在“上眼皮”及双腿浮肿;⑥现代社会是一个科技及资讯发的社会,各位病友会有智能手机、平板、电脑等,经过大约2个月移植病房的难忘生活(不能使用手机、平板电脑等),相信各位病友都在出院后有这样的念头:我出院后一定要刷刷微信、看看微博,告诉自己的亲朋好友有关在移植病房的经历。有以上想法都能理解,但请亲们注意:做任何事情都要适可而止,不要过度用眼、不要过度劳累,以免影响休息和自身免疫力的恢复。建议每天使用手机、平板、电脑及看电视的时间不要超过6小时。请亲们合理安排作息时间。上帝给了你双脚,就给了你去任何地方的自由。亲爱的病友,由于你是“玻璃人”,抵抗力非常低下,建议移植后禁足:不到人员拥挤、嘈杂的公共场所去(包括商场、饭店、餐馆、超市、车站等);不乘坐公共交通工具(包括公交车、出租车、快车、专车、火车、地铁、飞机、高铁等);远离建筑工地、装修装潢场所,建议居住地距离建筑、装修工地500米以上。提倡饭后在安静的小区、公园散步、健身等。从医学的角度来看,手比脚还要脏,这是因为我们的双手,每天都接触各种物品,而各种物品上存在各种“病原菌”。为预防感染的发生,请各位病友做到以下几点:①需要“饭前便后”洗手,特别是服药前。洗手,推荐各位病友使用“七步洗手法”,具体做法,各位亲,可求助于“度娘”:百度搜索;②避免整理旧物,旧书,翻看往日的照片、喜爱的杂志,以及发霉的物品,预防真菌感染;③不提倡打扫卫生、做饭、扫地、拖地等家务;④不提倡自己整理床铺、洗衣服等。本文系范志平医生授权好大夫在线(www.haodf.com)发布,未经授权请勿转载。
 范志平 主治医师 南方医科大学南方医院 血液科4.5万人已读
范志平 主治医师 南方医科大学南方医院 血液科4.5万人已读 - 引用 服用TKI慢粒患者能升级做父母吗?
随着靶向药物酪氨酸激酶抑制剂(以下简称TKI)的普遍应用,服用TKI药物的慢粒患者生存期接近健康同龄人,生活质量也显著提高,家庭的完整性是其中不可忽略的一部分。很多年轻的慢粒患者都会面对这样一个问题:“吃着TKI药物,还能拥有健康的孩子吗?下面我们来解答服药期间的生育问题。男性患者可以正常当爸爸服用TKI药物期间,极少数男性的精子数量和活性会减少,但是生育能力不会下降。成年男性慢粒患者可以正常生育,胎儿的畸形率与普通人相比没有提高。服用TKI的男性患者,不需要因为生育需求而停药。如果患者担心服药后精子数量减少影响受孕,可以在服药前将精子冷冻起来,为以后的生育做准备。女性患者服药期间怀孕了怎么办?相对来说,女性患者的生育限制就要多很多。首先,医生会建议服用TKI药物的女性患者避孕。因为调查显示,孕期服用TKI药物,可以增加流产的风险和胎儿畸形的发生,畸胎的概率接近10%,显著高于正常人。尤其是在怀孕前三个月,服用TKI药物的危险特别大。服药期间怀孕,应考虑到TKI药物对胎儿的毒性。如果发现怀孕时已经服药了,需要权衡药物对胎儿的影响,以及停药对妈妈疾病的影响,咨询有经验的医生,再决定胎儿的去留。正常生育后的患者需尽快开始服药,避免母乳喂养。因为药物会进入乳汁,对胎儿造成影响。本文系江倩医生授权好大夫在线(www.haodf.com)发布,未经授权请勿转载
江倩 主任医师 北京大学人民医院 血液病研究所1.1万人已读 - 引用 肝素诱导血小板减少症的抗凝剂治疗
直接凝血酶抑制剂可用于处理肝素诱导血小板减少症的直接凝血酶抑制剂包括阿加曲班和比伐卢定。两项前瞻性临床试验评估了阿加曲班在临床确诊的肝素诱导血小板减少症合并或未合并血栓患者中的作用。在初步试验中,在无血栓的肝素诱导血小板减少症患者(n=160)当中,与历史对照相比,阿加曲班显著降低了复合终点的死亡、截肢以及新的血栓事件的发生(38.8%对25.6%;P=.014)。在有血栓的肝素诱导血小板减少症患者(n=144)当中阿加曲班与对照组相比记录的复合终点没有显著差异。同样,来自第二个阿加曲班试验的结果显示,在无血栓的肝素诱导血小板减少症患者中(n=189)阿加曲班与历史对照相比显著降低了复合终点的发生率(28.0%对38.8%;P =.04),但是在有血栓的肝素诱导血小板减少症患者中(n=229)则未显著降低(41.5%对56.5%;P =.07)。在两个试验中都证明,与对照组相比,阿加曲班显著降低肝素诱导血小板减少症合并或未合并血栓两组患者中血栓导致的死亡发生率以及新的血栓发生率(P< .05)。阿加曲班被食品药物管理局批准用于肝素诱导血小板减少症的即时治疗。阿加曲班主要经肝脏代谢,并且在肝功能不全患者中观察到该药物的清除延长。用于脏器功能障碍的危重病人以及肝素诱导血小板减少症治疗的许多抗凝剂治疗性给药剂量常常低于制造商建议并且需要频繁监测。制造商推荐的阿加曲班剂量可能太高,尤其是用于治疗危重病人的肝素诱导血小板减少症。阿加曲班1μg/kg/min减量给药可能足以提供充分的抗凝。对于比伐卢定、另一个直接凝血酶抑制剂,当超药品说明书使用治疗肝素诱导血小板减少症以及合并肝和/或肾功能不全或危重病人的肝素诱导血小板减少症时,同样建议减量。尽管比伐卢定的一些药理学特征,包括肝素诱导血小板减少症半衰期短和酶代谢,但是在肝素诱导血小板减少症的情况下是有利的,有关其用于肝素诱导血小板减少症的资料有限。达比加群是一个直接凝血酶抑制剂经食品药物管理局批准用于降低非瓣膜性房颤患者卒中和系统性栓塞风险。该药物没有批准用于治疗肝素诱导血小板减少症,并且NCCN指南小组目前不推荐在癌症患者静脉血栓栓塞中使用达比加群。对于肝素诱导血小板减少症的即刻治疗专家组推荐一种直接凝血酶抑制剂作为首选治疗。已发表的肝素诱导的血小板减少症治疗试验中没有头对头比较不同直接凝血酶抑制剂的试验。治疗选择时应该考虑到临床医师的经验以及肝素诱导血小板减少症即时治疗药物的方便程度。阿加曲班应该避免用于肝功能衰竭和严重肾功能不全患者。磺达肝素在治疗当前无血栓事件的肝素诱导的血小板减少症方面选择磺达肝素超药品说明书使用作为胃肠外直接凝血酶抑制剂的一个备选方案也被收入在NCCN静脉血栓栓塞指南中。在此情形下使用磺达肝素的优势除了可皮下给予之外还包括当其与华法林同时使用时不延长国际标准化比值。尽管在需要抗凝逆转的情况下磺达肝素半衰期长是一个缺点,但是潜在获益可能包括高凝状态反跳风险降低。此外,与直接凝血酶抑制剂不同,磺达肝素的治疗应答监测通常不用活化部分凝血活酶时间试验,因此消除了与直接凝血酶抑制剂叠加时华法林相关活化部分凝血活酶时间延长的难题。磺达肝素已用于少量肝素诱导血小板减少症患者并且通常似乎是安全的。罕有磺达肝素应用与肝素诱导血小板减少症发生之间相关性的报告,尽管在大多数病例中既往有普通肝素或低分子肝素暴露史。对于肝素诱导血小板减少症并且无磺达肝素禁忌症患者建议应用磺达肝素,但只限于那些已经从最近的肝素诱导血小板减少症无血栓事件中恢复并且随时可出院但是在华法林治疗时仍不稳定者。该指南纳入磺达肝素作为肝素诱导的血小板减少症即刻治疗的一个2B级选择。华法林专家组反对在肝素诱导血小板减少症验前概率4T评分中或高患者中使用华法林治疗。对于正在接受华法林的患者,应该中止并使用维生素K逆转。在肝素诱导血小板减少症患者中不应该启动华法林除非血小板计数恢复,因为有皮肤坏死和/或静脉性坏疽的可能性,其可能是在肝素诱导血小板减少症极度激活凝血的情况下华法林引起的蛋白C水平降低所致。在血小板恢复以后(≥150000/mcL或当血小板恢复至基线时),华法林应该与一种直接凝血酶抑制剂或磺达肝素叠加至少5天;只有在INR已经达到预定目标范围(INR2-3)24小时以后才应该停止直接凝血酶抑制剂或磺达肝素。因为直接凝血酶抑制剂和华法林两者都降低凝血酶活性,同时给予直接凝血酶抑制剂和华法林会对活化部分凝血活酶时间和国际标准化比值两者的实验室测定产生联合效应。然而,与华法林单药治疗相比,同步治疗没有对维生素K依赖性Ⅹ因子活性产生额外影响。因此,在使用直接凝血酶抑制剂的情况下华法林的抗凝效果可能被低估。尤其是阿加曲班以及其它的直接凝血酶抑制剂,在联合华法林治疗期间可延长国际标准化比值。因为这3个直接凝血酶抑制剂中阿加曲班对凝血酶的亲和力最低,阿加曲班需要更高血浆摩尔浓度才能延长活化部分凝血活酶时间;因此,与其他的直接凝血酶抑制剂相比阿加曲班延长国际标准化比值更显著。因此在停止阿加曲班前应该达到更高的目标国际标准化比值。一旦停止直接凝血酶抑制剂,应该在2-6小时后重新检测国际标准化比值和活化部分凝血活酶时间以确定华法林单药治疗时国际标准化比值是否是治疗性的。在从联合阿加曲班治疗转换的时候可选择Ⅹ因子染色体水平(其不受直接凝血酶抑制剂的影响)监测华法林活性。华法林治疗的持续时间取决于肝素诱导血小板减少症是否伴有血栓。在肝素诱导血小板减少症合并血栓患者中,血栓事件特征决定治疗的持续时间(深静脉血栓3个月,肺栓塞6个月)。在肝素诱导血小板减少症无血栓患者中,建议华法林治疗至少1个月。【NCCN VTE 2015V1 综述部分P90】
张品良 主任医师 山东第一医科大学附属肿瘤医院 呼吸内科4616人已读 - 引用 血液科通俗演义之二:怀孕期间发现血小板减少怎么办?
怀孕期间发现血小板减少怎么办?很多孕妇在体检的时候都会发现血小板减少,事实上血小板减少是怀孕期间比较常见的现象,临床统计可以发现大约5-8%左右的孕妇会发生无症状性血小板减少。临床上妊娠期血小板减少的病因主要以妊娠相关性血小板减少和免疫相关性血小板减少(ITP)为主,虽然绝大多数是良性疾病,但是如果血小板减少严重,可以直接威胁到孕妇妊娠期和分娩过程的安全以及胎儿和新生儿的健康,因此需引起我们的高度重视。怀孕期间(妊娠期)血小板减少通常由哪些原因引起通常引起妊娠期血小板减少的原因有以下几种:(1)妊娠相关性,即前面我们提到的正常妊娠期由于血液稀释等因素导致的血小板减少,这种血小板减少多发生于妊娠的晚期,且血小板水平一般高于70*109/L,不会发生严重的出血等并发症;(2)免疫相关性血小板减少,即由于自身免疫因素导致的血小板减少,我们过去通常说的“特发性血小板减少性紫癜(ITP)”,通常分为两种情况,其一是既往明确诊断过ITP,妊娠期血小板减少加重,另一种情况是既往没有诊断或者没有发现ITP,妊娠期间因发现血小板减少确诊,这种情况的血小板减少可以在妊娠的任何时期发病;(3)药物相关性血小板减少,比如肝素或者其他引起血小板减少的药物,这种情况通常与患者接触的相关药物密切相关,可发生在妊娠任何时期;(4)妊娠相关病理性疾病导致的血小板减少,妊娠期间由于机体出现严重的免疫和激素异常,引起相关的病理生理改变时,血小板减少可以作为这一病理改变的重要表现,相关原因包括HELLP综合症、抗磷脂综合症、TTP/HUS、先兆子癇(专业名词,仅供医生参考);(5) 其他血液系统相关疾病,妊娠期间如果患者发生血液系统疾病,也可以引起血小板减少,常见原因如白血病、再生障碍性贫血等。怀孕期间(妊娠期)如果发现血小板减少该做哪些检查虽然妊娠期血小板减少的病因复杂,但对于大多数的血小板减少的孕妇,并不是一来门诊就诊医生就会安排骨髓检查,通常医生会详细询问患者的既往相关病史(比如以前有没有患过血液系统疾病,如ITP、再生障碍性贫血等;有没有近期使用过引起血小板减少的药物),并根据患者的综合病史和检查结果分析进行后续诊疗建议。通常情况下,血小板>50*109/L的患者,一般2-4周随访血常规即可。而对于血小板<30*109/L,且高度怀疑血液系统相关疾病的患者,除了密切监测血常规变化,骨髓检查也是必要的(这个骨髓指证和非妊娠的患者相同,骨髓检查的适应症和禁忌症对于孕妇和正常人之间没有差别)。怀孕期间(妊娠期)血小板减少对孕妇和胎儿有影响吗妊娠期如果血小板>30*109/L,患者发生出血的风险很低,对于胎儿的生长发育也不会产生影响,对于这部分患者,如果排除了病理性的因素,通常在临床上不会给予特殊的处理。如果血小板<30*109/L,通常需要给予治疗,此时孕妇可能会有出血的风险(虽然国外也有报道血小板低于<30*109/L的孕妇在分娩前不需要升血小板治疗,但是相关风险的权衡要十分慎重)。对于分娩期孕妇,血小板的水平对于孕妇的安全十分重要。分娩时血小板>50*109/L,无论是阴道自然分娩还是剖腹产都是相对安全的。而如果血小板<50*109/L,分娩过程中母亲出血的风险会比较大,同时发生新生儿血小板减少的几率会增高。怀孕期间(妊娠期)血小板减少该如何处理在排除了其他病理因素的前提下(后续主要针对的是妊娠期ITP),妊娠期如果血小板>30*109/L,通常在临床上不会给予特殊的处理。由于血小板减少后患者血液粘滞度会增加,因此在饮食上要注意避免高脂肪饮食。如果血小板<30*109/L,需要进行干预,通常应用的治疗包括静脉丙种球蛋白、糖皮质激素、血小板输注。有部分研究认为糖皮质激素可以在妊娠早期影响胎儿发育,因此主张妊娠前期避免激素治疗,这样对于比较严重的血小板减少的孕妇,可供选择的治疗方案就比较少。而由于静脉丙种球蛋白治疗ITP后疗效持续时间不长,因此导致治疗花费会很大。分娩期血小板减少的处理,主要是为了避免产妇在生产过程中严重出血以及新生儿血小板减少的发生,通常对于血小板>50*109/L的患者,由于相关出血的风险很小,通常不需要特殊处理。而当血小板<50*109/L时,建议在分娩前一周进行丙种球蛋白、糖皮质激素治疗,必要时分娩前一天输注血小板治疗,以确保分娩安全。妊娠期血小板减少患者生产后血小板会恢复吗对于妊娠相关性血小板减少的患者,在分娩后血小板会逐渐恢复到正常。对于妊娠期ITP患者,由于妊娠本身是引起ITP血小板减少加重的重要免疫诱因,因此部分患者分娩后血小板可能会逐渐上升,但也有部分患者血小板减少持续存在,此时治疗需按照ITP的治疗原则进行。而对于其他病因导致的血小板减少,其后续血小板恢复与否则需要根据其对应致病因素去除情况来决定。(本文大部分知识性内容来自UPTODATE相关知识点和文献)
6326人已读 - 引用 血管瘤血小板减少综合征( Kasabach-Merritt 综合征)
血管瘤血小板减少综合征( Kasabach-Merritt 综合征) ,由Kasabach、Merritt 二氏于1940 年首先报道,患者有巨大的血管瘤、血小板减少及紫癜等特点,多见于婴幼儿期,为先天性疾病。此综合征在血管瘤的婴幼儿的人群中仅占1 % ,但病死率达30 %以上。由于血管瘤巨大, 滞留大量血液, 可使患儿血容量减少引起贫血, 滞留和消耗大量血小板, 凝血因子Ⅱ、Ⅴ、Ⅷ 和纤维蛋白原, 引起凝血机制异常而有出血倾向。Kasabach2M errit t 综合征的治疗主要是消除血管瘤及控制出血。目前治疗方法有: (1) 糖皮素激素治疗, 常规剂量无效时, 可用大剂量地塞米松或甲基强的松龙; (2) 放疗: 剂量为100~ 150cGy次, 4~ 10 次为一疗程。因放疗可引起各种后遗症,如局部生长障碍、骨破坏、诱发恶变等, 故不宜常规应用; (3) 栓塞疗法, 适用于血管起源清楚的病例。此法虽可避免手术引起的出血并发症, 若栓塞不当可损伤重要脏器及组织的血供, 有时可引起难以控制的脓毒血症; (4) 在发生D IC 的不同阶段, 可分别应用抗凝及纤溶抑制剂; 出血严重时, 可输注血小板或新鲜全血。此外, 尚可应用局部压迫、干扰素等治疗。
王雷波 主治医师 宁波大学附属第一医院外滩院区 小儿外科5708人已读 - 引用 发热伴血小板减少综合征(SFTS)
发热伴血小板减少综合征(SFTS),是一种新出现的出血热,其首个病例出现在中国农村地区。SFTS 的病原体为SFTS病毒(SFTSV),是一种新型的布尼亚病毒科白蛉病毒属病毒。自2010年首次报道以来,中国已有11个省份发现大约2500例该病病例,平均死亡率为7.3%。2012年日本和韩国也曾有此病报道。Heartland 病毒,美国从 2 例患者体内分离出的基因与发热伴血小板减少综合征病毒极为相近的布尼亚病毒科白蛉病毒属病毒。SFTS不仅是中国公众健康的巨大威胁,也给全世界其他地方带来了巨大的威胁。SFTS 病毒可通过基因突变、重组和在蜱媒介及脊椎动物宿主内进行同源性重组而快速进化。目前尚无针对SFTS的特异性治疗,而预防SFTS 病毒感染和传播最重要的措施就是预防被蜱虫叮咬。2014 年 5 月 16 日,Lancet infect disease 在线发表了中国的 Quan Liu 博士等关于发热伴血小板减少综合征的综述。该综述旨在提供新出现的蜱传播病毒的分子学特征及生态学相关信息,并对 SFTSV 感染的流行病学、临床症状、发病机制、诊断、治疗及预防进行介绍。现将全文编译如下。一、概述2007年5月,中国河南省信阳市有3例伴有高热、胃肠道出血、腹痛、腹胀、恶心、呕吐和转氨酶升高的患者被当地一所医院诊断为急性胃炎。其中一例患者的亲属向河南省疾病预防和控制中心上报了此疾病。河南省 CDC 进行的专项调查发现此病临床特征为:急性起病,主要症状包括发热,白细胞及血小板数量减少,谷丙转氨酶、谷草转氨酶升高和蛋白尿。基于以上临床特征,河南省 CDC排除了胃肠道疾病的可能,并开始查找相似案例,结果发现2007年河南共出现79例该病病例,其中10例死亡(死亡率12.7%)。当时河南省出现由恙虫病东方体引起的恙虫病(丛林斑疹伤寒)暴发,河南省附近的安徽省也出现了由嗜吞噬细胞无形体引起的人粒细胞无形体病感染。这些疾病有相似的临床特征。因此,立克次体疾病(如人粒细胞无形体病,恙虫病)和由查菲埃立克体引起的人单核细胞埃里克体病被认为是此次河南疾病暴发的可能原因。然而,在206例可疑病例中仅有6例(3%)最后确诊为粒细胞无形体感染,并且2007年后的3年内均未分离出病原体。山东、江苏、湖北、安徽和辽宁也有SFTS的病例报道。2010 年,一种被称为 SFTS 病毒或布尼亚病毒的新型病毒从 SFTS 患者身上分离出来。此病毒被认为是中国发热伴血小板减少相关致命性疾病的病原体。2012年日本和韩国也曾有此病报道。美国密苏苏里州也有报道称他们从两名患发热伴血小板减少疾病的患者上分离出另一种白蛉病毒,Heartland病毒。Heartland病毒与SFTS病毒在基因上密切相关。此病溯源至美国2009年,日本、韩国2012年夏天,但是没证据证明这些患者曾到中国旅游。这些病毒可能有不同的起源,但是它们可引起相似的或甚至一样的症状和临床预后。新出现的SFTS 病毒的确起源于50-150年前的中国。也许这个病原体也曾在日本和韩国长时间出现过,Heartland病毒也在美国出现过。在本综述中,作者讨论了SFTS病毒的分子学特征及生态学信息,并描述了 SFTS 病毒感染的流行病学、临床症状、发病机制、诊断、治疗及预防。二、病原体1、分类SFTS病毒属于布尼亚病毒科白蛉病毒属。布尼亚病毒科在RNA病毒中所占比例最大,其包括超过350种病毒,可分成以下5个属:布尼亚病毒属、汉坦病毒属、内罗病毒属、白蛉病毒属和番茄斑萎病毒属。除了汉坦病毒属是由啮齿类动物传播外,其它布尼亚病毒科病毒均由节肢动物媒介传播。布尼亚病毒科病毒可感染不同种类的动物和植物,该科的许多病毒可引起人类发热性感染,包括脑炎及出血热。由于布尼亚病毒在人类宿主及地域分布上的发病率增加,其被认为是威胁公众健康的重要的新发病原体。白蛉病毒属病毒包含有大约70种抗原性不同的血清型,分成白蛉热病毒组和乌库尼米病毒组两组。白蛉热组病毒通过白蛉或蚊子传播,乌库尼米组病毒通过蜱传播。从遗传学角度来说,SFTS 病毒应该归类至白蛉病毒属,但是它不同于白蛉病毒属内其他两组已知的病毒,所以它可能是白蛉病毒属内的第三组病毒。虽然SFTS病毒和Heartland病毒与乌库尼米病毒组其他成员的序列相似性有限,但是它们仍被归类至乌库尼米病毒组,因为他们在M片段缺乏非结构小蛋白,但是它们有特定的血清学特征并且均以蜱作为常见的节肢动物传播媒介。Matsuno及其同事已经辨别出白蛉病毒属内一组新的病毒—Bhanja组病毒,其包括Bhanja,Forecariah和Palma病毒。相对于乌库尼米病毒组,SFTS病毒和Heartland病毒与Bhanja病毒组的关联更密切。2、基因及结构SFTS病毒颗粒呈球形,直径约80-100nm,外有脂质包膜,表面有长5-10nm的多肽棘突。SFTS病毒基因组由三个小、中、大负链RNA片段组成。小RNA片段有1744个核苷酸,通过双向方式编码核蛋白和非结构蛋白。3’和5’端的非翻译区域高度保守,形成一个锅柄状结构。核蛋白包装基因组RNA至核糖核蛋白复合体以保护其免受外源性核酸酶或宿主细胞免疫系统的降解。尽管核蛋白功能相似,但是SFTS 病毒核蛋白的晶体结构可加工成稳定的六聚体环状结构以协助病毒RNA包衣入壳,这是病毒复制中关键的一步。小RNA片段中的四个残基,A8、F11、A25及L28,对病毒的寡聚作用至关重要,其与布尼亚病毒科的其他成员有着非常大的区别。此外,核蛋白对RNA转录、复制和病毒组装有活化作用。SFTS 病毒的核蛋白和非结构蛋白均能通过抑制干扰素β和核因子κB信号通路的活化来抑制宿主细胞的抗病毒免疫反应。中RNA片段有3378个核苷酸,其包含了编码糖蛋白前体1073个氨基酸的单个开放阅读框,这对病毒组装、病毒颗粒的形成及粘附至新的靶细胞上均有至关重要的作用。糖蛋白缠绕至细胞表面蛋白的非肌型肌球蛋白重链IIA上,对SFTSV早期感染的效率有一定作用。大RNA片段有6368核苷酸,编码2084个氨基酸的大蛋白—病毒RNA依赖的RNA聚合酶,此酶促进病毒RNA的复制和转录。其N末端的流感样核酸内切酶区域对病毒鸟苷帽依赖性转录有重要作用。3、基因多样性不考虑SFTS 病毒广阔的地域分布,尽管分离所得的SFTS 病毒有超过90%的序列相似,其仍可分成A至E 5个亚系。从动物(狗、猫、羊、水牛和家牛)分离所得的为A亚系,其不表现出地理区域群聚特征,这与其他狂犬病病毒及汉坦病毒等人畜共患病毒不同。在Bhanja组病毒中Heartland病毒和SFTSV有共同的病毒祖先。SFTS 病毒基因多样性的分子机制目前尚未完全阐明,但是有数个研究提示病毒可通过基因突变、自然重组和同源性重组获得快速进化。由于SFTSV的RNA依赖的RNA聚合酶无校对功能,SFTSV在复制过程中有较高的突变率(每年每个位点约10-4次替换),这是其基因多样性的基础。重组是分段性基因组病毒中一个非常有效的进化力量,与病毒的高致病力及媒介与宿主间的传播有关系,甚至可以导致新的疾病暴发。自然重组的遗传进化证据曾在白蛉病毒属的成员中报道过,如裂谷热病毒和坎第鲁病毒。Ding等已经在小片段中辨别出有重组的两种SFTSV病毒株,这提示重组是推动SFTSV快速变化的力量。虽然在负链RNA病毒中同源性重组很罕见,但是其已经在SFTSV的中片段及其他负链RNA病毒如流感病毒、埃博拉病毒和汉坦病毒中被发现,这提示在病毒快速进化中基因间重组起一定作用。SFTSV的蜱传播媒介长角蜱和脊椎储存宿主可为病毒的同源性重组和自然重组的共同感染提供位置。4、流行病学2009年7月SFTS首次在中国河南省和湖北省的乡村地区被报道。实际上,第 1 例病例于2006年9月发生在安徽省滁州市定远县。2009年6月至2010年9月,河南、湖北、山东、辽宁、安徽和江苏省共有171名患者确诊为SFTS 病毒感染。2012 年年底前,此病已在以下 11 个省份中发现:河南、湖北、安徽、山东、江苏、浙江、江西、广西、云南、陕西、辽宁。2011年-2012年,中国共有2047例SFTSV感染(其中有129例死亡),感染主要分布在中国东部和中部的206个县。河南、湖北和山东的病例数最多,分别占总数的48%、22%和16%。血清监测提示丘陵地区1.0%-3.8%的检测人群有SFTSV抗体,这表明SFTSV已经在中国广泛的流动,并且仅很小一部分感染人群发病。SFTS的发病率从湖北的千分之0.03至山东的千分之0.05不等。中国以外的第一个病例于2009年出现在北韩。2012年南韩确诊一例致死病例,2013 年报道了 6 例该病病例,其中 4 例患者死亡。日本在 2013 年 4 月报道了 11 例该病病例,其中 7 例患者死亡,其明显增多的病例数似乎局限于当地,而不是从中国传播过去。美国首次注意到此病是在 2009 年,当时美国西北部密苏苏里州的两名农民因高热、疲倦、腹泻、血小板和白细胞减少而入院治疗,两名农民均在起病前 5-7 天被蜱虫叮咬过。在中国,SFTS 病毒感染的总死亡率大约是7.3%(2391例病例,174例死亡),其他研究中的死亡率为6.3%-30.0%。疾病流行区的农民是主要的风险人群,中国97%的SFTS患者为居住在森林和丘陵地区或在农田工作的农民,许多患者在发病前7-9天曾被蜱虫叮咬。疾病的潜伏期一般为7-14天,平均9天。SFTS病例主要分布于年龄为35-80岁的蜱暴露人群。在河南省SFTS主要在采茶季节的四月份和五月份发生。野外活动,如露营和登山,也是接触蜱虫的潜在风险因素。SFTS病例主要在春天和夏天出现零散式增加。直接与受感染的血液或血性分泌物接触可引起感染,此前曾有小群体感染报道,这提示SFTS疾病存在人传人的传播方式。医院护理人员、患者亲属及陪同人员是第二种主要的易感人群,他们主要通过与患者的血性分泌物接触而感染。虽然无证据证明病毒可引起动物感染,但是来自亚临床病毒感染动物的血液可能是感染的一个来源。因此,兽医和屠宰场工人也处于感染风险中。5、生活习性⑴传播媒介作为一种新发现的白蛉病毒,研究人员认为SFTS 病毒是一种节肢动物传染病毒,这意味着病毒可通过不同种类的媒介传播。在中国,SFTS 病毒曾在长角血蜱(流行率2.1%-5.4%)上被发现,此长角血蜱是从SFTS患者所住地方的家养动物身上收集得到。从长角血蜱身上分离所得病毒的RNA序列与患者身上分离所得的SFTSV序列密切相关。SFTS 病毒也曾在流行区和非流行区的微小牛蜱上被发现,但是微小牛蜱上SFTS 病毒的携带率要低于长角血蜱(0.6% vs 4.9%)。流行区内的长角血蜱病毒携带率高于非流行区提示长角血蜱是SFTS 病毒传播的主要媒介。长角血蜱和牛脾在中国和其他国家广泛分布,所以在这些地区的蜱上进行SFTS 病毒检测是有必要的。从流行区的黑线姬鼠和山羊上收集的革螨和恙螨也曾发现SFTS 病毒,所以这两者也是潜在的传播媒介。Heartland病毒曾在美洲钝眼蜱的幼虫上发现并分离获得,此美洲钝眼蜱幼虫从一名患者的农场和附近的农耕保护区获得。这些发现提示通过病毒寄生宿主的喂食蜱幼虫被感染,并且在春天和夏天通过幼虫寻找寄生宿主的途径病毒被传播至人类。因此,美洲钝眼蜱也被认为是 Heartland 病毒的传播媒介。SFTS 病毒和 Heartland 病毒目前仍未在蚊子身上发现,白蛉病毒目前也还没被研究。⑵脊椎储存宿主研究认为SFTS 病毒在地方性蜱-脊椎动物-蜱链中循环。虽然目前无证据证明SFTS 病毒可引起动物发病,但是基于核蛋白双抗原夹心ELISA法进行SFTSV血清阳性筛选的调查已经在家养动物中进行。在山东省,羊群的血清阳性率为75-95%,家牛为57%,狗为52%,家鸡为36%。江苏省,家鸡血清阳性率为1%,猪为5%,狗为6%,家牛为32%,羊群为57%。在湖北省,狗的血清阳性率为55%,羊为67%,家牛为80%。病毒RNA,特别是低水平的RNA,仅在被调查的一小部分动物中被检测到(1.7%-5.3%)。这些研究结果提示,家养动物是SFTS病毒传播扩大的主要宿主,通过给家养动物喂食蜱可扩大SFTS 病毒的传播。除了家养动物,许多野生动物,如鹿、刺猬、鼬鼠、刷尾负鼠和一些鸟类,均是蜱的常规宿主。啮齿类动物上也曾发现SFTS 病毒感染,感染率从姬鼠的7%至小家鼠和褐家鼠的8%。在美国的明尼苏达州,SFTS 病毒核蛋白的抗体阳性率在山羊上是11%,绵羊为13%,家牛为16%,白尾鹿为12%,麋鹿为18%。因此,这个区域的所有家养动物和圈养农场动物均暴露于SFTS 病毒或Heartland病毒。三、临床特征SFTS以发热和呼吸道或消化道症状急性起病,随后出现血小板和白细胞数进行性下降。典型的SFTSV感染分为四期:潜伏期,发热期,多器官功能衰竭期和恢复期。潜伏期为蜱虫叮咬后5-14天。潜伏期的长短可受病毒剂量和感染途径等多个因素影响。接触或暴露于患者的血液或血性分泌物至发病的平均天数为大约10天(7-12天)。发热期以流感样症状为特征,如突发高热(38-41℃)并持续5-11天,头痛,疲乏,肌痛,及纳差、恶心、呕吐、腹泻等消化道症状,同时伴随着血小板和白细胞减少,淋巴结肿大。这个时期可检测到高病毒载量,是临床诊断的一个重要标志。多器官衰竭期以重症患者的多器官功能进行性下降或存活者的自限性恢复为特征。多器官衰竭发展迅速,首先累及肝脏和心脏,然后是肺和肾脏。多器官衰竭期可与发热期重叠,大部分病例在发病的5天后进入多器官衰竭期并持续7-14天。在多器官衰竭期,存活者的血清病毒载量逐渐下降,但是在死亡患者中病毒载量仍很高。在器官衰竭期,死亡患者体内重要的生物标志物水平(如谷草转氨酶、肌酸激酶、乳酸脱氢酶和CK-MB)均明显高于存活者。出血、神经系统症状、DIC、多器官衰竭和持续的血小板数下降等临床症状提示病重,死亡风险大。多器官衰竭期非常重要,因为此期存活下来的患者最终可获得康复。从发病至死亡的平均时间是9天。大部分患者(85%)预后良好,但是既往有基础疾病、出现精神症状、有出血倾向、低钠血症或为老年患者,临床预后较差。存活者的恢复期在发病后11-19天开始。此时临床症状开始消退,实验室检查逐渐恢复正常。血小板减少(<100×109/L)和白细胞减少(<4.0×109/L)似乎是 SFTSV 感染始终如一的特征,这可能是因为外周器官损伤或循环抗体对血小板的损伤在增加。SFTS 患者也会出现谷丙转氨酶、谷草转氨酶、乳酸脱氢酶和肌酸激酶升高。在所有患者中也会观察到凝血功能紊乱,其导致 DIC,最后出现多器官衰竭。存活者在 3-4 周内生化检查恢复至正常。病毒复制和宿主的免疫反应可影响 SFTS 的严重程度和临床预后。重症患者与非重症患者实验室检查与死亡关系密切指标包括:血 RNA 病毒载量等于或高于 105拷贝 /ml,凝血酶原时间等于或长于 65.1 秒,活化部分凝血酶原时间等于或长于 62.6 秒,谷丙转氨酶等于或高于 288U/L。死亡病例中磷脂酶 A、纤维蛋白原、肝脏抗菌多肽、IL-6、IL-10、干扰素γ和趋化因子 IL-8 等急性时相蛋白水平均明显高于存活者。Lu等发现老年患者、意识水平下降、乳酸脱氢酶升高及肌酸激酶升高是预测患者高死亡风险的阳性指标,这些患者在治疗中应更加慎重。表 1 发热伴血小板减少综合征患者的临床症状四、发病机制SFTS的发病机制目前未完全清楚。布尼亚病毒科病毒常见的致病特点是:能抑制宿主的免疫反应,以病毒的快速复制和多器官衰竭为特征。Sun等分析了SFTS患者的免疫功能。发现SFTS患者的CD3+T细胞和CD4+T细胞的数量明显低于正常人,而NK细胞的比例升高,尤其是在重症SFTSV感染的急性期。免疫功能的抑制可使患者身体条件恶化,增加继发性感染的风险。NK 细胞通过产生干扰素γ、肿瘤坏死因子(TNF)α,IL-10 和粒细胞集落刺激因子(G-CSF)等细胞因子来发挥免疫调节功能。这些细胞因子的水平与疾病的严重程度相关。产生干扰素β是宿主固有免疫系统对抗病毒感染的一个防御机制。然而,在 SFTS 患者血中几乎检测不到干扰素β。在 SFTS 病毒感染的单核细胞内,与干扰素β相关的转录因子适当上调,但是 TNF 受体相关因子 3 和 6 及线粒体抗病毒信号蛋白这些下游分子水平无改变或下调,因此抑制了干扰素β的诱生。此外,SFTS 病毒编码的核蛋白和非结构蛋白等蛋白抑制了干扰素β启动子和核因子κB 信号的活化。这些抑制效应也能在其他布尼亚病毒上发现。炎症因子在病毒所致疾病的发病机制中起着重要作用。当初次免疫反应不能抑制病毒复制时,病毒可诱导靶细胞释放过量的细胞因子,从而导致病理性损伤。几种促炎性细胞因子以细胞因子风暴形式异常表达,这与SFTS的严重程度有关。细胞因子的不平衡表达有三种不同的模式。IL-1受体拮抗剂、IL-6、IL10、G-CSF、干扰素γ诱导蛋白和单核细胞趋化蛋白 1 在 SFTS 中表达增加,并且常见于重症患者多于非重症患者。相反,血小板来源生长因子和 RANTES(调节活化和正常 T 细胞表达的因子)水平下降。在患者康复期这些细胞因子恢复至正常水平。IL-1β、IL-8 和巨噬细胞炎症蛋白 1α、1β仅在 SFTS 重症患者中表达增加,但是在存活者的恢复期中这些因子表达也增加。这些细胞因子与血清病毒载量和各种临床特征有关。例如,单核细胞趋化蛋白 1 和 IL-8 对进行性肾损伤有重要意义,IL-1 受体拮抗剂和 IL-6 与流行性肾病有关,单核细胞趋化蛋白 1 和干扰素γ诱导蛋白可导致肝脏炎症和纤维化,IL-8 可增加血管通透性。RANTES低表达与病毒所致疾病的严重程度有关。SFTS 患者中 RANTES 与血小板来源生长因子低表达可能是由于循环中血小板数量减少,外周循环中的血小板是这两种细胞因子的主要来源。SFTS中的出血热症状也与 TNFα增高有关。TNFα作用于内皮细胞,诱导血管舒张物质产生,并刺激一氧化碳合成,增加毛细血管内皮细胞通透性。SFTS 病毒能粘附至血小板上,这可被脾巨噬细胞识别并吞噬,导致血小板减少,这是 SFTS 一个常见的临床表现。SFTSV 可在多种细胞类型中进行复制,但是其主要的靶目标是网状细胞。受感染的单核细胞几乎是完整的且不凋亡,它们能够保持持续的病毒复制,这是因为其通过淋巴管播散至血循环中,引起初次病毒血症。虽然 SFTS 病毒可劫持巨噬细胞进行病毒复制,但是在小鼠模型中巨噬细胞可抑制病毒生长并最终将其清除。因此,免疫力强的患者可将 SFTS 病毒清除,但是在免疫抑制的患者中病毒可有效增殖并导致多器官功能障碍或患者死亡。五、诊断早期诊断SFTS 病毒感染对患者的存活及预防病毒传播均有关键作用。目前SFTS主要依据流行季节、地域分布、蜱虫叮咬史、临床表现和实验室检查(血小板和白细胞减少)等流行病学特征来诊断。由于SFTS的临床表现不具有特异性,所以实验室检查很必要。鉴别诊断包括出血热伴肾病综合征、登革热、血小板性紫癜、伤寒、钩端螺旋体病和人边虫病。SFTS病毒分离应在生物安全三级实验室进行。SFTS 病毒可感染多种细胞系,包括Vero、Vero E6、L929和DH82,但是其仅在DH82和Vero E6细胞内引起细胞病变。在培养的细胞中分离病毒简单而快速(2-5天),但是病毒可能还没诱导细胞病变或仅有一点病变,所以必须通过电子显微镜和分子学或血清学方法对病毒致病进行确认。RT-PCR是确诊SFTS 病毒感染的一种高度特异、敏感且快速的实验室方法。全自动实时PCR方法的出现使得SFTS 病毒检测比传统RT-PCR检测污染率更低,敏感性和特异性更高,检测更快速。目前多重实时RT-PCR可同时检测四种出血热病原体—SFTSV、汉坦病毒、汉城病毒和登革热病毒。等温扩增技术也可用于检测SFTS 病毒 RNA,包括RT环介导等温扩增和RT交叉引物扩增。这些方法均具有高特异性和敏感性。虽然SFTS 病毒感染可产生高滴度病毒血症,便于病毒分离和分子检测,但是持续时间很短,一般在发病后1-6天。在发病后大约7天可在血中检测到SFTS 病毒的特异性抗体。特异性IgG在感染5年后仍可检测到,但是IgM在感染后4个月就检测不出。新近的SFTS 病毒感染可通过检测IgM抗体, IgG抗体血清转换,或者抗体滴度至少升高4倍来进行诊断。目前也有几种用于检测病毒抗体的血清学方法,包括血清中和试验,间接免疫荧光检测和ELISA。血清中和试验是金标准,但是其费力、价格昂贵并且需要活病毒来操作。因此,血清中和试验仅能在配置高级别生物安全设备的特殊实验室进行。ELISA检测价格低廉、耗时少,且目前已研究出一种重组、基于核蛋白的双抗原夹心ELISA方法用于检测人类和动物体内的SFTS 病毒抗体。此方法比血清中和试验敏感性高,并且其在SFTS 病毒和登革热病毒或汉坦病毒中无交叉反应。六、治疗由于目前尚无SFTS 的特异性治疗,所以应尽早对SFTS患者开展对症治疗和支持治疗。卧床休息,流质或半流质饮食,补充充足的水分。如果患者不能进食或处于危重状态,必需补充能量和水分以确保患者水电解质平衡,尤其对于低钠血症患者。发热患者应给予物理降温,必要时使用退热药。对有明显出血或血小板数很低(<30×109/L)的患者推荐输注血小板和血浆。如果患者中性粒细胞数量严重减少,应给予 G-CSF。合并细菌或者真菌继发性感染的患者应给予合适的抗生素或抗真菌药。心理学干预有助于患者康复。目前已经批准利巴韦林用于几种病毒感染的治疗,包括布尼亚病毒属裂谷热病毒和克里米亚刚果热病毒。虽然利巴韦林在体外试验中可抑制病毒活动,但是在重症或非重症患者住院期间其对血小板数量或病毒载量无明显影响,所以利巴韦林在治疗 SFTS 病毒感染上作用甚微。抗体在多种病毒所致疾病的治疗中有着重要作用,例如汉坦病毒、巨细胞病毒和狂犬病病毒。其作用机制包括中和作用、激活补体、抗体依赖的细胞毒性和调理作用。给予患者中和抗体可降低病毒载量,预防病毒传播,同时可能降低预后不良的风险。从噬菌体抗体库中分离所得的人单克隆抗体 4-5 在体外试验中对 SFTS 病毒有中和功能,其或许能用于处于高风险人传人传播如医院职工和患者亲属等人群中以预防病毒感染。血浆交换和利巴韦林法成功治疗了两名快速进展至 SFTS 的患者,这表明血浆交换和利巴韦林可作为治疗重症 SFTS 患者的潜在救命疗法。七、预防目前尚无针对SFTS 病毒的疫苗,所以居住在疾病流行区域的居民应该重视以下预防措施:避免被蜱虫叮咬,包括避免去森林和草丛茂盛、落叶堆积的灌木丛,尤其在蜱虫活跃季节,因为这些地方蜱虫很多;检查人或动物皮肤表面是否有蜱虫;使用DEET或百灭宁等驱虫剂。在暴露的皮肤上涂抹包含20%或以上剂量DEET的驱虫剂可保护数小时,百灭宁处理过的物品如衣服、靴子和帐篷等可在清洗70次以上仍有保护作用。Vaughn和Meshnick指出,百灭宁浸泡过的衣物可有效抵抗蜱虫叮咬,与标准防护措施相比,其可降低93%的蜱虫叮咬发生率。可能暴露于病毒血液的人们应该采取实用性保护措施,包括戴手套和穿保护性衣物以避免直接接触受感染的组织或血液。SFTS患者应该进行隔离,直至血中未再检测出病毒,与这些患者接触的每个人均应监测是否有发热,直至潜伏期结束。SFTS 病毒对酸、热、乙醚、脱氧胆酸钠和其他常见的消毒剂及紫外线照射敏感,可被这些物质快速灭活。污染了患者血液、分泌物和排泄物的物品表面应该进行消毒。对于处于高感染风险的人群,如通过接触或针刺伤直接暴露于SFTS患者血液的人群,可给与利巴韦林口服或皮下注射人单克隆抗体进行预防。八、未来的研究方向SFTS 病毒和Heartland病毒的流行区环境和传播链的动态变化应更进一步阐明。应详细描述气候因素、储存宿主和媒介的作用,野生动物中 SFTS 病毒感染的血清转换也还需要进一步研究。从中国、日本、韩国和美国分离所得病毒的比较研究应阐明这些病毒的起源和多样性。同时,应该采取包括疫苗、抗病毒药物、治疗性抗体或免疫血清等有效措施来预防和控制病毒感染。有关病毒复制的新消息或许能促进新药物的研究。有关病毒出血热发病机制的进一步研究将会为DIC和多器官功能衰竭的发病机制指明方向。了解SFTS 病毒感染或其他病毒出血热的新机制将会促进新的治疗分子学的研究。由于SFTS的传播链很复杂,其脊椎动物宿主和传播媒介蜱时刻处于变动的环境中,所以SFTS很难控制和预防。我们应该重视一人健康即全民健康方法在这种新兴的蜱传播人畜共患疾病中的作用。
揭盛华 主任医师 武汉协和医院 感染科1.6万人已读 - 引用 血小板减少之日常生活九细则
知道血小板减少后,大多患者都会过得“小心翼翼”,如:不再剧烈运动、不再肆无忌惮的吃饭、不再偷偷地享受毛毛雨等等。我们为什么要这么谨慎呢?究其原因就是血小板太低,容易造成出血。出血时对身体的危害比较大,易造成不可逆转的伤害。出现血小板减少后我们我们需要在哪些方面注意呢?1、 避免感染:特别是儿童,本身这些孩子免疫力要比正常孩子低一些。很容易出现交叉感染。提醒孩子在学校等公共场所要特别注意远离其他生病的孩子,避免感冒。2、 药物的应用:我们常说有些药物对血象会造成影响,无论何种原因就医时都要及时告知主治医生你的病情,避免造成不知情用药造成血小板病情加重的情况。如:感冒、发热等。3、 避免外伤:一般血小板>50x109/L时,除严重创伤外一般不会出血;PLT在20-50x109/L轻度创伤就可引起出血;PLT<20x109/L出血风险较大,应避免剧烈运动,卧床休息,如有出血请及时到当地医院就诊。4、 避免便秘:防止大便干燥引起肛裂导致出血。5、 避免吃太硬、纤维素长的食物:在血小板特别低的时候,需要注意不要吃太硬、纤维素长的食物,避免造成口腔及消化道黏膜的损伤引起出血。6、注意月经量:女性患者在血小板特别低的时候,容易出现月经量多或经期过长的情况,日常需要多注意观察,如有月经异常需要及时就诊。7、 避免鼻腔干燥:鼻腔粘膜干燥,容易出现鼻腔出血。血小板减少患者要格外注意,避免鼻出血不止。8、 怀孕及分娩:孕期要定期检查血常规,在血小板特别少时要进行对症治疗。妊娠后期要提前住院,为分娩准备,减少分娩时出现的危险,产后也要住院一段时间观察母婴双方的身体状况。9、 避免手术:血小板数值太低时避免手术等有创治疗,比如拔牙,痔疮等等治疗,可先使用药物治疗将数值稳定在安全范围,再考虑进行手术治疗。血小板减少患者预防出血,是避免病情进一步加重的重要手段。日常生活中不忽略这些小细节,对预防出血有积极的意义。
刘风 主任医师 中国中医科学院西苑医院 血液科6490人已读 - 引用 血栓性血小板减少性紫癜的诊断和治疗进展
血栓性血小板减少性紫癜(thrombotic thrombocytopenic purpura,TTP)是一组微血管血栓出血综合症,是一种高致死、高风险的临床急诊,及早诊断并启动血浆置换(plasma exchange,PEX)有效改善预后,提高生存率。主要临床特征包括微血管病性溶血性贫血、血小板减少、神经精神症状、发热、肾脏受累等。发病机制与VWF(血管性血友病因子)金属蛋白裂解酶ADAMTS13严重缺乏、血管内皮细胞VWF释放异常、血小板异常活化等有关。临床分为遗传性TTP(ADAMTS 13基因突变,导致酶活性下降或缺乏)和获得性TTP[1]。应该说,TTP的诊断和治疗极富挑战,因为:1)诊断标准并不精准;2)不通过血浆置换生存率仅为10%;3)尽管PEX可使80%的患者存活,但面临众多PEX相关并发症的高危性[2]。临床上存在对该病认识不足延误诊断;或过度担心PEX并发症而延误最佳治疗时机;或过分依赖ADAMTS13活性的检测;抑或过度诊断TTP而采取过度治疗等实际问题。本文联系临床实际结合文献,谈些自己的体会。一一、 获得性TTP复杂多变,鉴别诊断尤为重要。确切说,TTP是成人微血管病性溶血、血小板减少伴或不伴有神经和肾脏异常的通用名。获得性TTP分为特发性TTP(存在ADAMTS 13自身抗体,即检测到ADAMTS13抑制物)和继发性TTP(诸如感染、药物、肿瘤、自身免疫性疾病、造血干细胞移植、妊娠等因素诱发,预后差)。前者治疗以PEX及免疫抑制剂为主,后者关键则是尽快去除原发因素。TTP诊断所谓 “三联征”(微血管病性溶血性贫血、血小板减少、神经精神症状)、“五联征”(微血管病性溶血性贫血、血小板减少、神经精神症状、肾损、发热)虽为人们所熟知,但据此临床真正做出疾病最初评估和处理却相当困难。首先,临床实践中经典的“五联征”几乎很难见到,大多患者仅表现为微血管病性溶血性贫血和血小板减少,神经和肾脏异常并不常见,发热较罕见[2]。其次,临床上发现患者存在微血管病性溶血性贫血和血小板减少的证据,一般都不难考虑到TTP存在的可能,但在短时间内判断特发性TTP或是继发性TTP;排除诸如溶血尿毒综合症(HUS)、弥漫性血管内凝血(DIC)、HELLP 综合征、Evans 综合征、妊娠、子痫等疾病伴发的微血管病性溶血性贫血和血小板减少,实属不易[3]。正因为如此,引发治疗决定困难。特别是特发性TTP,及早确诊、及时启动关键性治疗PEX及免疫抑制剂是救治成功的决定性因素。因此,临床一旦诊断明确或高度怀疑TTP,无论轻重,都应尽快积极治疗(包括PEX、糖皮质激素等);同时尽快筛查致病因素,及时修正治疗方案(如败血症相关的TTP必须以强有力的抗感染为主,而非PEX或是免疫抑制治疗)[1~3]。二二、 正确认识ADAMTS13检测的意义1997年有人首次证明慢性复发性TTP与血浆中存在异常巨大VWF多聚体相关,随后很快发现TTP患者存在VWF大小主要调节子ADAMTS13的严重缺陷,而VWF多聚体大小的调节在预防自发微血管血小板聚集很重要,是TTP的主要病理生理产物[4]。我们知道,获得性ADAMTS13缺乏往往由于循环血中抗ADAMTS13自身抗体活性或ADAMTS13清除增加。ADAMTS13活性的检测也因此一度被作为TTP诊断和治疗评估的重要指标。经过10多年的临床观察研究,大多学者认为ADAMTS13 的活性测定对初始治疗决定可能并无帮助;尽管严重的ADAMTS13缺乏(<10%< span="">)是TTP特征之一,但它对于启动或撤减PEX的决定既不足够敏感,也非特异[2]。George JN等的研究表明并不是所有严重ADAMTS13缺乏的患者都能确定为TTP[2,3]。一组65例严重ADAMTS13缺乏的患者中,6例在开始PEX后发现存在其他疾病,其中5例有全身感染(包括造血干细胞移植患者),1例尸检后诊断为卡波西肉瘤[5]。严重ADAMTS13缺乏的TTP患者存在复发危险,尤其是缓解后1年内最常见,预期7.5年复发危险为41%,而没有严重ADAMTS13缺乏的患者复发罕见。因此,临床可根据患者初次发作时ADAMTS13缺乏的严重程度推测今后复发可能性,以期加强监测血小板计数,及时发现复发苗头,及早干预,减少TTP相关并发症。ADAMTS13活性检测在TTP缓解后预测复发价值的相关临床资料提示许多患者在康复后持续或间歇性ADAMTS13缺乏。41例严重ADAMTS13缺乏的患者缓解期间接受了1~4次的ADAMTS13活性检测,结果发现7例(17%)ADAMTS13活性<10%< span="">,19例(46%)<50%< span="">,9例(22%)存在ADAMTS13抑制物。说明缓解期严重ADAMTS13缺乏与TTP临床症状并无关联,其临床重要性与复发的危险性并不肯定。认为TTP康复后并不需要常规进行ADAMTS13活性检测[3]。总之,对ADAMTS13作用的认知有助于对TTP发病机制的理解,而初始评估和处置决定仍主要取决于临床判断。三三、 强调TTP综合治疗的重要性TTP发病急、进展快,治疗棘手。关键在于权衡TTP诊断的可能性是否足以规避PEX治疗的风险。有资料显示高滴度抗ADAMTS13抗体是TTP治疗相关并发症和死亡率的高危因素。临床上有时在来不及寻找TTP的病因学时必须做出PEX的治疗决策,诸如可疑药物相关 的TTP等稍有耽搁就可能出现神经异常、肾功能衰竭或死亡,明确病因后再作治疗策略调整。近几年的临床实践发现不伴有严重ADAMTS13缺乏的患者PEX治疗同样有效,提示PEX能替换ADAMTS13缺乏的血浆,清除自身抗体的假设并不适用于所有患者。血浆输注在开始PEX前能短暂获益,为进一步治疗赢得时间。开始PEX治疗后,下一步就是决定是否启用糖皮质激素,并根据患者病情的严重程度调整激素使用剂量。目的在于抑制抗ADAMTS13活性的自身抗体,强化PEX疗效,严重ADAMTS13缺乏的患者获益较明显。若患者不可能存在ADAMTS13缺乏,如严重的急性肾衰,或存在药物相关TTP或大肠杆菌感染相关TTP的病史和临床特征,则不主张使用激素治疗。激素治疗后ADAMTS13抑制物持续阳性的特发性TTP,可加用长春新碱、环磷酰胺、环孢菌素等免疫抑制剂,以期减少自身抗体产生,控制病情进展。静脉用丙种免疫球蛋白可用于PEX无效或多发复发的患者[1~3]。复发难治性特发性TTP,也可加用抗CD20单抗(利妥昔单抗,美罗华),推荐用美罗华 375mg/m2/周×4周。近期有研究报道利妥昔单抗也可能作为常规的初始治疗,但仍存在病人选择和分析方面的问题,例如未采用盲法、对照组治疗匹配不理想、每组随访时间不定、缺乏RFS(无复发生存)资料,不是所有患者均存在严重ADAMTS13缺乏等,因而缺乏说服力[5]。另外,现有资料表明仅采用PEX和糖皮质激素治疗使许多伴有严重ADAMTS13缺乏的患者取得及时缓解,并且大多不再复发,因此也不能说明利妥昔单抗的应用价值。关于TTP患者输注血小板的风险,生物学原理显而易见,临床应慎用。也有人报道血小板输注的副作用也并不明显:33/54例(61%)严重ADAMTS13缺乏的患者接受1次或多次的血小板输注(大多在考虑或建立TTP诊断前),结果发现接受或未接受血小板输注的患者在死亡率和严重神经事件的发生率方面没有区别。因此认为TTP患者若存在严重血小板减少和明显出血或需要进行侵入性治疗措施等情况下同样适合输注血小板,但中心静脉导管植入并没有必要输注血小板[2]。也就是说,对于TTP患者而言,严重的血小板减少本身并不是血小板输注的指证,但在预防或处理TTP伴发的出血时输注血小板并没有观察到更多的副作用。 四四、 及时发现复发并控制是TTP治疗成功的关键TTP复发定义为首次发作完全缓解30天后再发生TTP临床表现,发生率约30~40%,多在疾病首次发作后的1年内。遗传性TTP及ADAMTS13抑制物阳性的特发性TTP易复发。定期随访监测血小板计数极为重要,是TTP治疗和复发评判的主要指标;初发TTP患者ADAMTS 13活性检测有助于预后判断;对ADAMTS13抑制物持续阳性者需注意疾病复发。目前大多专家并不主张针对预防TTP复发的维持治疗。有人认为急性发作时加用美罗华有望减少疾病复发[2,6]。一般来说,由于加强监控,及早识别复发并及时治疗,TTP复发治疗的生存优于初发患者。综上所述,TTP经典的临床五联征表现极少看到,许多患者仅存在血小板减少和微血管病性溶血性贫血,首次发作诊断困难;PEX是TTP治疗首选,同时要注意寻找可能的致病因素,一旦发现原发因素,应以治疗原发疾病为主;辅助性糖皮质激素治疗以及选择性应用利妥昔单抗,可减少获取疾病缓解所需时间及PEX次数,从而避免PEX治疗相关的并发症;TTP恢复后的细致随访极为重要。参考文献:1. 阮长耿 余自强 血栓性血小板减少性紫癜诊断与治疗中国专家共识(2012版) 中华血液学杂志,2012;33(11):983~9842. George JN, Al-Nouri ZL. Diagnostic and therapeutic challenges in the thrombotic thrombocytopenic purpura and hemolytic uremic syndromes. ASH Education Program Book, 2012;604~6093. George JN. How I treat patients with thrombotic thrombocytopenic purpura. Blood, 2010;116(20):4060~40694. Kremer Hovinga JA, Lmmle B. Role of ADAMTS13 in the pathogenesis, diagnosis, and treatment of thrombotic thrombocytopenic purpura. ASH Education Program Book, 2012;610~6165. Scully MF, McDonald V, Cavenagh JD, et al. A phase 2 study of the safety and efficacy of rituximab with plasma exchange in acute acquired thrombotic thrombocytopenic purpura. Blood. 2011;118(7):1746~1753.6. Kremer Hovinga JA, Vesely SK, Terrell DR, et al. Survival and relapse in patients with thrombotic thrombocytopenic purpura. Blood. 2010;115(8):1500~1511.
沈群 主任医师 江苏省中医院 血液科7131人已读






